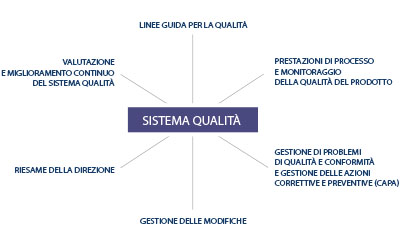
Elementi fondanti del sistema qualità
Il sistema di qualità integrato di Aspen è costituito dagli elementi chiave di seguito elencati; i requisiti normativi regionali, i principi GMP applicabili e le aspettative di Aspen in materia di gestione della qualità per tutte le tipologie di prodotti possono essere adattati in modo flessibile in ogni fase del ciclo di vita.
LINEE GUIDA PER LA QUALITÀ DI ASPEN
Tali importanti elementi costitutivi assicurano la costante fornitura di prodotti di alta qualità da parte di Aspen e garantiscono al Gruppo la leadership di settore per quanto riguarda la conformità ai requisiti di qualità e normativi basata su innovazione, ricerca scientifica e probabilità di rischio.
Le politiche e gli standard di qualità del Gruppo Aspen, che descrivono i requisiti per la produzione e la fornitura a livello commerciale, includono le norme GMP applicabili, i requisiti di qualità di Aspen e le conoscenze derivate dai diversi ambienti normativi in cui operiamo. L'approccio di Aspen allo sviluppo e al mantenimento dei nostri standard di qualità garantisce il mantenimento dei principi fondamentali di qualità di Aspen, indipendentemente dal tipo di prodotto, dalle tecnologie utilizzate per la sua realizzazione o dal mercato a cui è destinato.
Gli standard di qualità di Aspen sono a loro volta utilizzati per sviluppare SOP e/o procedure conformi per i singoli stabilimenti, riguardanti prodotti commercializzati o destinati all'uso clinico. Il rispetto di tali standard è obbligatorio e viene monitorato attraverso il programma di audit del Gruppo.
PRESTAZIONI DI PROCESSO E MONITORAGGIO DELLA QUALITÀ DEL PRODOTTO
Aspen valuta la performance di processo e la qualità del prodotto attraverso revisioni periodiche dei prodotti approvati («Periodic Product Reviews», PPR). Tra le fonti per l'acquisizione dei dati figurano i risultati dei test condotti sui prodotti, i dati di stabilità, i reclami, le non conformità e le indagini. I dati vengono analizzati per verificare se i processi sono coerenti e per individuare eventuali opportunità di miglioramento della qualità. Le misure raccomandate possono essere affrontate attraverso la gestione delle modifiche e/o azioni correttive e preventive («Corrective and Preventive Actions», CAPA).
GESTIONE DI PROBLEMI DI QUALITÀ E CONFORMITÀ E GESTIONE DELLE AZIONI CORRETTIVE E PREVENTIVE (CAPA)
I potenziali problemi di qualità e conformità sono identificati attraverso numerose fonti, tra cui audit interni, non conformità e indagini «fuori specifica», indagini su reclami o analisi del divario di conformità (valutazione delle registrazioni dei prodotti, valutazione dei risultati delle ispezioni delle autorità normative e analisi delle tendenze dei dati pertinenti raccolti da tali fonti). Gli standard globali di Aspen rispecchiano questo processo completo, che garantisce l'analisi di tali problemi di qualità e conformità o di tendenze confermate per determinare l'eventuale impatto sulla qualità del prodotto e la causa principale del problema. Sia che il problema si verifichi presso uno stabilimento Aspen o la sede di un appaltatore, si applicano opportune misure CAPA per ridurre o prevenire le possibili ripercussioni del problema sul consumatore o sul paziente. Le CAPA sono gestite e monitorate al fine di garantire la rapida applicazione delle misure e la valutazione della loro efficacia.
GESTIONE DELLE MODIFICHE
Aspen garantisce che le modifiche proposte che potrebbero potenzialmente incidere sulla qualità del prodotto siano valutate da esperti del settore, affinché sia assicurato che tale modifica sia giustificata da un punto di vista tecnico/specialistico e venga valutata in relazione all'immissione in commercio e/o alle attuali conoscenze del prodotto o del processo. La modifica proposta sarà inoltre esaminata ad un livello adeguato del sistema di gestione della qualità, a seconda dell'entità e delle sue potenziali ripercussioni. La valutazione comprende l'identificazione di tutte le misure necessarie per sostenere l'attuazione della modifica, al fine di confermare che gli obiettivi della stessa sono stati raggiunti e dimostrare che essa non incide negativamente sulla qualità del prodotto.
RIESAME DELLA DIREZIONE
Un processo di notifica della direzione facilita la tempestiva escalation dei problemi correlati alla qualità e di natura normativa/di conformità relativi ai prodotti commercializzati e per uso clinico, attraverso un sistema di notifiche sequenziali o concomitanti.
Ogni unità operativa di Aspen organizza incontri interfunzionali per esaminare la qualità dei prodotti approvati, che includono la presenza di rappresentanti delle aree di produzione, analisi, tecnologia, qualità e catena di fornitura, a seconda del caso.
VALUTAZIONE E MIGLIORAMENTO CONTINUO DEL SISTEMA QUALITÀ
 Aspen garantisce la trasparenza e la responsabilità a livello dell'intero Gruppo, management incluso, in relazione alle performance del sistema qualità, attraverso la definizione e la comunicazione di una serie di parametri chiave per la qualità. Tali parametri vengono valutati periodicamente dalla politica per la qualità del Gruppo, al fine di identificare le aree di miglioramento e assegnare ai team di progetto le attività da svolgere in tali aree.
Aspen garantisce la trasparenza e la responsabilità a livello dell'intero Gruppo, management incluso, in relazione alle performance del sistema qualità, attraverso la definizione e la comunicazione di una serie di parametri chiave per la qualità. Tali parametri vengono valutati periodicamente dalla politica per la qualità del Gruppo, al fine di identificare le aree di miglioramento e assegnare ai team di progetto le attività da svolgere in tali aree.
La revisione periodica e il miglioramento continuo del sistema qualità include anche il monitoraggio dei fattori chiave interni ed esterni, comprese le nuove normative, linee guida e questioni relative alla qualità, nonché i cambiamenti nel contesto aziendale. Tale revisione promuove il miglioramento continuo nell'ambito dell'intero Gruppo.


 America Latina Spagnola
America Latina Spagnola Canada
Canada Francia
Francia Germania
Germania Mauritius
Mauritius Paesi Bassi
Paesi Bassi Australia
Australia Cina
Cina Filippine
Filippine Giappone
Giappone Malaysia
Malaysia Taiwan
Taiwan Ethicare
Ethicare Beta Healthcare
Beta Healthcare Kama
Kama Nigeria
Nigeria Shelys
Shelys
 Ghana-Kama
Ghana-Kama  Kenia-BETA HEALTHCARE
Kenia-BETA HEALTHCARE  MAURITIUS
MAURITIUS  Südafrika-FCC
Südafrika-FCC  Südafrika-HOLDINGS
Südafrika-HOLDINGS  Südafrika-Pharmacare
Südafrika-Pharmacare  Tansania-SHELYS
Tansania-SHELYS  KANADA
KANADA  China
China  Malaysia
Malaysia  Philippinen
Philippinen  DEUTSCHLAND
DEUTSCHLAND  FRANKREICH
FRANKREICH  NIEDERLANDE
NIEDERLANDE  Niederlande-Aspen API
Niederlande-Aspen API  Russland
Russland